ДАЙДЖЕСТ НОВОСТЕЙ ЗА 27.08. - 10.09.
(Разработан РКЦ ЦЭ совместно с Фондом Росконгресс.)
- 9 сентября Малайзия представила первые в регионе Национальные этические руководящие принципы по биотехнологии — шаг, который не только определяет внутреннюю политику страны, но и задает новый стандарт для всей АСЕАН. Разработанные Министерством науки, технологий и инноваций (MOSTI), эти принципы формируют комплексную рамочную структуру, направленную на развитие экологической устойчивости в генной инженерии, исследованиях клеточных культур и искусственного интеллекта.
- 28 августа международный журнал Cell опубликовал прорывную работу, выполненную командой ученых из Института геномики Huada (BGI) совместно с рядом ведущих медицинских центров Китая. Исследование посвящено новой версии технологии пространственной транскриптомики — Stereo-seq V2, которая решает одну из фундаментальных проблем современной молекулярной медицины: невозможность детального анализа широко распространенных клинических образцов, сохраненных методом FFPE (формалин-фиксированные, парафин-заливные).
- С 26 августа по 2 сентября китайская биотехнологическая компания Bloomage Biotech, мировой лидер по производству гиалуроновой кислоты, опубликовала пять новых патентов на рекомбинантный коллаген. Они охватывают типы III, IV и XVII коллагена, включая методы их создания и применения. Особое значение имеет патент на рекомбинантный XVII тип коллагена, ключевой для поддержания стабильности стволовых клеток кожи и фолликулов. Число патентов компании в области рекомбинантного коллагена достигло семи, что свидетельствует о системной стратегии освоения данной технологии.
- 1 сентября ученые из Египта представили новое достижение в области зеленой биотехнологии: из вод Красного моря был выделен уникальный штамм бактерий, способный эффективно производить щелочную протеазу на дешевом сырье из отходов соевого производства. Данное исследование открывает путь к более доступному и экологичному производству данного промышленного фермента, используемого в пищевой, кормовой, кожевенной промышленности и других сферах.
- Ученые из Университета Персидского залива (Иран) разработали новый способ создания наночастиц для потенциального применения в лечении рака. Исследование, опубликованное 2 сентября в журнале Scientific Reports, направлено на создание безопасного и эффективного агента для современных методов борьбы с опухолями — фототермической и фотодинамической терапии.
- 8 сентября в крупнейшем городском лесном массиве — государственном парке Педра-Бранка (Рио-де-Жанейро) — бразильские ученые обнаружили новый вид мух, способный стать важным инструментом в борьбе с тропическими болезнями и сохранении экосистемных услуг. Новый вид, получивший научное название Hemerodromia mystica, описан в журнале International Journal of Tropical Insect Science и представляет собой редкий пример естественного биологического контроля.
РАЗДЕЛ I: Институциональное развитие и регуляторная система биоэкономики
1. Малайзия строит этическую основу для биоэкономики: первый стандарт АСЕАН
9 сентября Малайзия представила первые в регионе Национальные этические руководящие принципы по биотехнологиям — шаг, который не только определяет внутреннюю политику страны, но и задает новый стандарт для БРИКС и АСЕАН. Разработанные Министерством науки, технологий и инноваций (MOSTI), эти принципы формируют комплексную рамочную структуру, направленную на развитие экологической устойчивости в генной инженерии, исследованиях клеточных культур и искусственного интеллекта.
Документ объединяет 15 этических принципов: уважение к автономии и человеческому достоинству, защита генетических данных, прозрачность клинических исследований, гуманное обращение с животными, сохранение биосуверенитета, устойчивое использование природных ресурсов и забота о будущих поколениях. Особое внимание уделяется инклюзивности — данные принципы ориентированы не только на ученых и фармацевтические компании, но и на законодателей, педагогов и общественные организации. Они разработаны как «живой документ», подлежащий регулярному пересмотру в связи с быстрым развитием технологий — от редактирования генома до лабораторного выращивания мяса, которое может изменить глобальные продовольственные цепочки. Такой подход призван предотвратить дисбаланс между технологическим потенциалом и общественным доверием, который уже стал препятствием для внедрения биотехнологий в ряде стран.
Малайзия, глава Подкомитета по биотехнологии АСЕАН, использует этот документ как платформу для региональной координации. На двухдневном семинаре «Navigating Bioethical Frontiers: Sustainability and Resilience in ASEAN» собрались более 250 экспертов из всех государств АСЕАН, Международного центра генетической инженерии и биотехнологий и других международных организаций. Обсуждались темы, выходящие за рамки медицины — от этики использования ИИ в диагностике до интеграции традиционных знаний коренных народов в биоресурсные системы. Это свидетельствует о переходе от узкоспециализированной биотехнологии к системному пониманию биоэкономики на стыке науки, культуры, права и экологии.
Ключевым достижением стало новое понимание этичности не как ограничения, но непременного условия устойчивости. Без доверия общества к безопасности и справедливости новых продуктов, будь то генетически модифицированные культуры или персонализированные терапии, инновации рискуют столкнуться с сопротивлением, регуляторными барьерами и потерей легитимности. Малайзийская модель демонстрирует, что долгосрочная конкурентоспособность в биоэкономике зависит не столько от скорости НИОКР и патентования, но и от качества институциональных механизмов этического использования.
Данный подход особенно значим для стран Юго-Восточной Азии с высоким биоразнообразием, богатыми традициями в использовании природных ресурсов и быстро растущим сектором биотехнологий. Принятие единых этических стандартов помогает предотвратить «этический арбитраж» (перемещение исследований в страны со слабым регулированием) и способствует формированию инклюзивного биоэкономического пространства, в котором прогресс не противопоставляется социальному или экологическому процветанию.
РАЗДЕЛ II: Биотехнологические прорывы и диагностические технологии
2. Китайская технология Stereo-seq V2 раскрывает скрытую жизнь старых медицинских образцов
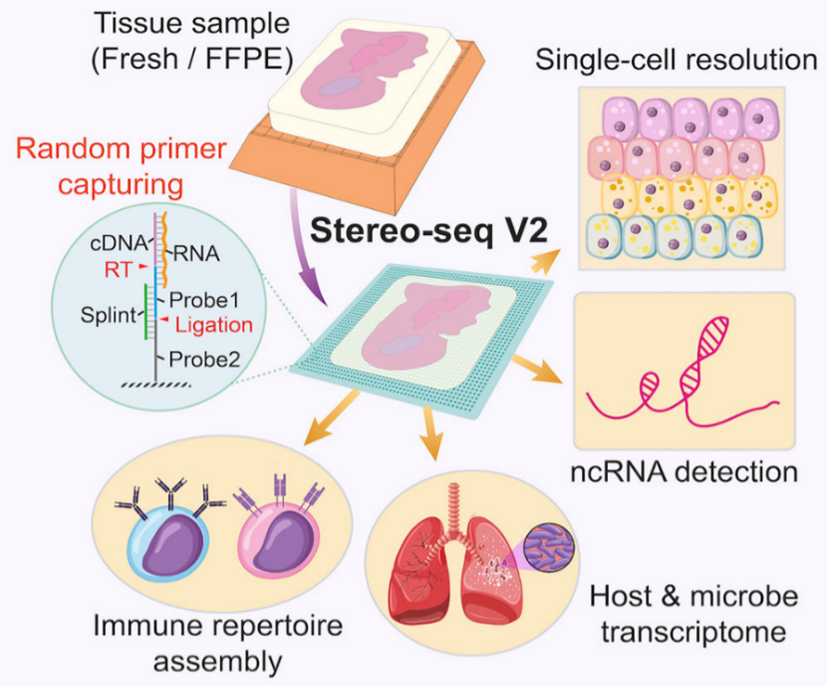
Рис. 2. Принцип работы Stereo-seq V2. Источник: Cell
28 августа международный журнал Cell опубликовал прорывную работу, выполненную командой ученых из Института геномики BGI совместно с рядом ведущих медицинских и научных центров Китая. Исследование посвящено новой версии технологии пространственной транскриптомики — Stereo-seq V2, которая решает одну из фундаментальных проблем современной молекулярной медицины: невозможность детального анализа широко распространенных клинических образцов, сохраненных методом FFPE (формалин-фиксированные, парафин-заливные).
FFPE — стандартный способ сохранения биопсийного и операционного материала, применяемый в патологоанатомических отделениях по всему миру уже более ста лет. Миллионы таких образцов, содержащих информацию о раковых опухолях, инфекционных процессах и других заболеваниях, хранятся при комнатной температуре. Однако формалин, необходимый для долгосрочной стабилизации тканевой структуры, вызывает химические модификации и разрушение РНК, что значительно затрудняет молекулярный анализ таких образцов.
Stereo-seq V2 представляет собой комплексный подход, основанный на двух ключевых инновациях: усовершенствованный де-кросслинкинг и случайный захват РНК. Команда разработала специальный химический протокол, который эффективно разрывает ковалентные связи, создаваемые формальдегидом между белками и нуклеиновыми кислотами, тем самым восстанавливая доступность РНК без ее дальнейшего деградирования. Вместо использования поли-T-примеров, которые ловят только мРНК с поли-A хвостом, технология применяет случайные праймеры. Это позволяет одновременно захватывать широкий спектр РНК-молекул, включая не только мРНК, кодирующие белки, но и длинные некодирующие РНК (lncRNA) и малые ядерные РНК (snoRNA), играющие важную регуляторную роль. После захвата РНК, молекулы помечаются пространственными штрих-кодами, что позволяет с высокой точностью определить их исходное местоположение в ткани. В результате создается пространственный «атлас» — детализированная карта активности генов в трехмерной структуре органа или опухоли.
Применение Stereo-seq V2 продемонстрировало высокие возможности в области анализа опухолей: на образцах рака молочной железы ученые смогли четко визуализировать границы между зонами опухолевого роста, иммунного ответа и участками некроза. Были выявлены различные субпопуляции раковых клеток и обнаружены специфические события альтернативного сплайсинга — процесса, когда один и тот же ген может порождать несколько вариантов белка, тесно связанных с прогрессированием болезни или устойчивостью к терапии.
Ключевое достижение — способность технологии одновременно анализировать как человеческие клетки, так и патоген. В исследованиях на модели туберкулеза у мышей и в человеческих легочных тканях удалось точно нанести на карту пространственное распределение бактерий Mycobacterium tuberculosis. Более того, впервые были идентифицированы скопления специфических B-клеточных клонов вокруг очагов инфекции и прослежен процесс их созревания — когда антитела становятся все более эффективными против возбудителя.
3. Новые патенты на рекомбинантный коллаген от Bloomage Biotech
Рис. 3. Источник: TuChong
С 26 августа по 2 сентября китайская биотехнологическая компания Bloomage Biotech, мировой лидер по производству гиалуроновой кислоты, опубликовала пять новых патентов на рекомбинантный коллаген. Они охватывают типы III, IV и XVII коллагена, включая методы их создания и применения. Особое значение имеет патент на рекомбинантный XVII тип коллагена, ключевой для поддержания стабильности стволовых клеток кожи и фолликулов. Число патентов компании в области рекомбинантного коллагена достигло семи, что свидетельствует о системной стратегии освоения данной технологии.
Рекомбинантный коллаген, синтезируемый с помощью генной инженерии, обладает рядом преимуществ перед животными источниками: точный контроль молекулярной массы, структуры и биосовместимости, что делает его идеальным для высокоточного применения, от гемостатиков до инъекционных филлеров. Bloomage Biotech с 2021 года активно развивает эту область, инвестируя в НИОКР и реализуя государственные проекты. Уже сегодня собственные сырьевые компоненты компании применяются в медицинских повязках и косметических продуктах.
Особое внимание привлекает разработка «коллагеновых инъекций» — на середину 2025 года данное изделие на основе рекомбинантного человеческого коллагена находится на стадии клинических испытаний как медицинское устройство III класса. Это является важным этапом на пути к коммерциализации, поскольку в Китае все инъекционные процедуры («водные уколы») с 2022 года определены в III класс, для которого действуют более строгие процедуры регистрации и клинических испытаний. Ранее, в апреле 2025 года, Bloomage Biotech уже получила одобрение на свой первый продукт класса III — инъекционный раствор на основе гиалуроновой кислоты с лидокаином для улучшения качества кожи.
Эта активность не является заменой основного бизнеса, а представляет собой стратегическое расширение компании в рамках подхода «двойного развития», где рекомбинантный коллаген дополняет гиалуроновую кислоту. Директор компании Чжао Янь заявляла о намерении сделать коллаген вторым стратегическим биоактивным веществом после гиалуроновой кислоты. Хотя рынок рекомбинантного коллагена пока менее зрел, чем гиалуроновая кислота, его потенциал огромен: по прогнозам к 2030 году китайский рынок может достичь более 200 млрд юаней, а глобальный — вырасти с 1,2 млрд долл. США в 2024 году до 3,8 млрд долл. США к 2033 году. В этом контексте патентная активность Bloomage Biotech воспринимается как попытка занять доминирующие позиции в новом, быстрорастущем сегменте биоэкономики.
РАЗДЕЛ III: Зеленые биопроцессы и устойчивое производство
4. Египет: оптимизация производства щелочной протеазы из уникального штамма бактерий Красного моря
Рис. 4. Источник: Charles River Laboratories
1 сентября ученые из Египта представили новое достижение в области зеленой биотехнологии: из вод Красного моря был выделен уникальный штамм бактерий, способный эффективно производить щелочную протеазу на дешевом сырье из отходов соевого производства. Данное исследование открывает путь к более доступному и экологичному производству данного промышленного фермента, используемого в пищевой, кормовой, кожевенной промышленности и других сферах.
Щелочные протеазы — одни из самых востребованных ферментов в мире, благодаря своей способности расщеплять белки, использующиеся в стиральных порошках и гелях для разрушения пятен; в пищевой промышленности для производства сыров, гидролиза белков сои и получения биологически активных пептидов; в кожевенной и кормовой промышленности. Группа ученых из Национального исследовательского центра Египта обнаружила микроорганизмы, способные производить высокие количества протеаз при минимальных затратах. Исследователи собрали образцы морской воды на глубине 15 метров у побережья г. Рас-Судр (Египет) и выделили из данных проб три штамма бактерий, способных вырабатывать протеазы. С помощью анализа генетического «паспорта» бактерий ученые определили, что штамм принадлежит виду Bacillus amyloliquefaciens, широко известному своей способностью выделять ферменты. Новый штамм получил название NRC-IB-11, а его генетическая последовательность зарегистрирована в международной базе данных GenBank под номером PP034178.1.
Особый акцент в исследовании был сделан на использовании агропромышленных отходов в качестве питательной среды для бактерий. Исследователи проверили, на каком из шести доступных органических отходов бактерия будет производить больше всего фермента. В эксперименте участвовали: обезжиренный жмых миндаля, куриные перья, обезжиренный льняной жмых, шелуха креветок, пшеничные отруби, обезжиренный соевый жмых. Лучшим субстратом оказался последний — побочный продукт при производстве соевого масла. На этой среде бактерия NRC-IB-11 выработала 476 единиц фермента на мл (U/mL) — значительно больше, чем на других отходах.
После этого ученые оптимизировали условия культивирования: концентрацию субстрата, объем посевного материала, pH, температуру и скорость перемешивания, благодаря чему удалось повысить выход фермента до впечатляющих 590 U/mL — одного из лучших показателей для подобных систем. Весь процесс происходил в однокомпонентной среде, то есть без добавления дополнительных питательных веществ, что снижает себестоимость производства.
Новый штамм Bacillus amyloliquefaciens NRC-IB-11 особенно интересен тем, что он производит фермент при умеренной температуре (35 °C), хорошо работает в сильнощелочной среде (pH 10) и обладает устойчивостью к солям и высокому содержанию минералов в силу своего происхождения. Согласно оценкам авторов, использование единственного компонента — соевого жмыха — позволило снизить себестоимость производства фермента на 30%. Ученые уже предлагают дальнейшее исследование штамма с помощью редактирования генов или усиления экспрессии фермента для достижения большей эффективности.
5. Иран: «зеленый» синтез наночастиц для лечения рака

Рис. 5. Процесс синтеза наночастиц. Источник: Nature
Ученые из Университета Персидского залива (Иран) разработали новый способ создания наночастиц для потенциального применения в лечении рака. Исследование, опубликованное 2 сентября в журнале Scientific Reports, направлено на создание безопасного и эффективного агента для современных методов борьбы с опухолями — фототермической и фотодинамической терапии.
Исследователи разрабатывали биосовместимые наночастицы оксида железа (α-Fe2O3), известные как гематит, с использованием экологически чистых методов синтеза и стабилизировали их природным полисахаридом — хитозаном. Такой подход позволяет избежать использования токсичных химикатов и повышает вероятность безопасного применения наночастиц для человеческого организма.
Исследователи использовали комбинированный метод, объединяющий «зеленый» синтез и гидротермальный процесс. Зеленый синтез подразумевает использование безвредных веществ для получения наноматериалов, в данном случае — хитозана, биополимера, получаемого из панцирей крабов и других морских обитателей. Хитозан не только послужил «зеленым» агентом для восстановления и формирования частиц оксида железа, но и выступил в роли стабилизатора, предотвращая их слипание и обеспечивая однородность суспензии. Гидротермальный метод позволил точно контролировать размер и форму наночастиц за счет нагревания раствора в герметичном сосуде под давлением. Полученный нанокомпозит CS-α-Fe2O3 был тщательно изучен с помощью рентгеновской дифракции и инфракрасной спектроскопии для подтверждения его состава и структуры.
Главным достижением стало то, что созданные наночастицы показали хорошие свойства для фототермической терапии. Этот метод заключается в том, что наночастицы, попав в область опухоли, поглощают свет лазера и преобразуют его в тепло, уничтожая раковые клетки. Эффективность этого процесса оценивается по коэффициенту фототермического преобразования: для нанокомпозита он составил 7%, что свидетельствует о способности наночастиц генерировать значительное количество тепла при лазерном облучении и подтверждается экспериментами по повышению температуры раствора.
Авторы отдельно отмечают потенциал своего нанокомпозита и для фотодинамической терапии, когда специальное вещество (фотосенсибилизатор) вступает в реакцию с кислородом под воздействием света и образует активные формы кислорода, губительные для клеток. Для подтверждения данного эффекта необходимо проведение дальнейших испытаний.
Создание безопасных и эффективных наноагентов для фототермической и фотодинамической терапии — одна из важнейших задач современной онкологии. Эти методы являются минимально инвазивными и могут целенаправленно уничтожать опухоли, минимизируя повреждение здоровых тканей по сравнению с химиотерапией или лучевой терапией. Использование биополимера хитозана значительно повышает их биосовместимость и снижает токсичность, что является критически важным для клинического применения. И хотя данное исследование находится на доклинической стадии, оно открывает путь к разработке новых терапевтических стратегий.
РАЗДЕЛ IV: Поддержание биоразнообразия для здравоохранения
6. «Супермуха» Бразилии: природный биоконтроллер для устойчивого здравоохранения

Рис. 6. Источник: LABORATÓRIO INTEGRADO / FIOCRUZ
8 сентября в крупнейшем городском лесном массиве — государственном парке Педра-Бранка (Рио-де-Жанейро) — бразильские ученые обнаружили новый вид мух, способный стать важным инструментом в борьбе с тропическими болезнями и сохранении экосистемных услуг. Новый вид, получивший научное название Hemerodromia mystica, описан в журнале International Journal of Tropical Insect Science и представляет собой редкий пример естественного биологического контроля.
Эта крошечная муха (длиной всего 3 мм) является хищником, специализирующимся на личинках и куколках черных мошек (Simulium spp.) — кровососущих насекомых, переносчиков онхоцеркоза (речная слепота) и кишечного шистосомоза. В отличие от многих хищных насекомых, H. mystica проявляет необычную стратегию развития: она использует пустые куколки своих жертв как укрытие для собственной стадии куколки — явление, известное как инквилинизм. Это означает, что новая особь не убивает жертву напрямую, а «занимает» ее защитную оболочку, чтобы завершить метаморфоз. Такой механизм ранее не был зафиксирован в Неотропической зоне, что делает открытие уникальным с точки зрения эволюционной экологии.
Помимо хищнической роли, H. mystica играет функцию биоиндикатора: как и другие представители своего рода, она требует для размножения чистые, хорошо аэрированные водотоки. Т.о., ее присутствие в парке становится показателем хорошего качества воды и низкого уровня загрязнения, что особенно ценно в условиях урбанизации. Ученые подчеркивают, что наличие данного вида в Рио-де-Жанейро является хорошим сигналом, поскольку означает, что водосборные бассейны под защитой, а экосистемы сохраняют функциональность.
Сочетание хищничества по отношению к векторам болезней и чувствительности к качеству окружающей среды делает Hemerodromia mystica идеальным кандидатом для интеграции в практики эко-управления здоровьем и природоподобных технологий. В условиях роста устойчивости к инсектицидам у комаров и мошек, а также растущих затрат на медицинскую помощь, такие природные механизмы обретают стратегически важное значение. Использование H. mystica как элемента биоконтроля поможет снизить зависимость от химических средств, уменьшить экологический след программ борьбы с заболеваниями и одновременно укрепить охрану водных ресурсов.
Открытие также демонстрирует, что даже в пределах крупных городов продолжают существовать сложные и тонко сбалансированные экологические взаимодействия. Атлантический лес, один из самых биоразнообразных биомов планеты, остается хранилищем невиданных форм жизни, потенциально решающих глобальные задачи здравоохранения и экологической безопасности. Hemerodromia mystica — живое свидетельство того, как сохранение биоразнообразия напрямую трансформируется в экономические и социальные выгоды.
